經濟實惠、健康無公害的FMD無疑是一個聯合治療肝癌好搭檔
發布時間:
2022-02-14
來源:
作者:
閱讀數:
這年頭,管住嘴也能治病,也就是飲食干預療法。
而在這飲食干預療法中,模擬禁食飲食(FMD)可是香餑餑!
FMD以低水平碳水化合物和蛋白質、相對較高脂肪為特征,從而限制熱量為標準飲食的50%及以下。近些年,已有不少動物實驗證實(推薦閱讀:動物造模), FMD能夠延長小鼠壽命,減少和延遲癌癥的發生、緩解自身免疫性疾病、調節腸道菌群等[1-4]。
基于此,FMD藥物研發、FMD與其它藥物的聯合治療等也博得了科學家們的關注,以期為臨床治療提供一種方便又有效的策略。
前不久,一篇發表在Science Advances期刊上的論文提出,FMD與肝細胞癌(HCC)的靶向藥——索拉非尼,在治療HCC中具有協同作用。(推薦閱讀:Hep-3B人肝癌細胞、HLE人肝癌細胞、RH-35大鼠肝癌細胞、Li-7人肝癌細胞、FAO大鼠肝癌細胞)
來自奧地利格拉茨大學的Andreas Prokesch和他的同事們發現, FMD不僅能加強索拉非尼的療效,還能改善索拉非尼的耐藥性問題,而這種協同作用依賴于抑癌基因p53的正常表達[5]。
肝癌是最常見的惡性腫瘤之一,是我國第5大常見癌癥,也是第2位腫瘤致死病因。在原發性肝癌中,HCC占75%-85%,是肝癌的主要形式[6]。
對于不可通過手術切除治療的HCC來說,索拉非尼是一種常用藥。這種抗腫瘤血管生成的靶向藥物能夠將總生存期延長3個月。然而遺憾的是,由于耐藥性的問題難以克服,在臨床上尚未出現索拉非尼單藥治療痊愈的病例[7,8]。
如此看來,索拉非尼在HCC治療上亟需尋找新出路。而經濟實惠、健康無公害的FMD無疑是一個聯合治療好搭檔。
這次,Prokesch和他的同事們就對索拉非尼與FMD的聯合療法進行了考察。
首先,他們選用了一種對索拉非尼具有很強耐藥性的HCC細胞——人肝癌細胞系HepG2,皮下注射給小鼠(NMRI)。并隨機分為4組進行不同治療,分別為安慰劑+隨意飲食組、安慰劑+FMD組、索拉非尼+隨意飲食組、索拉非尼+FMD組。
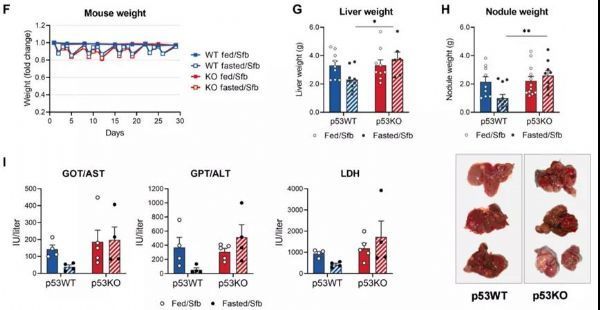
在用FMD喂養小鼠時,研究者們選擇了5:2斷食方案(每周斷食2天),而不是隔日斷食。他們發現,雖然兩種FMD方案都會導致小鼠短期內血糖水平以及體重下降,但如果小鼠采用5:2斷食方案喂養,體重從長期來看處于穩定狀態;而采用隔日斷食方案喂養的小鼠,體重呈不可挽救的下降趨勢,長期治療的話,怕是病還沒好鼠鼠就餓沒了。
經過超4周的治療,研究者們發現,索拉非尼或FMD的單一治療僅顯示出腫瘤減小的趨勢,腫瘤大小未發生明顯改變。與之相比,當聯合治療時,療效疊加,索拉非尼+FMD組小鼠的腫瘤生長被顯著抑制,且總體重未受影響。
這表明,FMD或能以協同效應減輕索拉非尼的耐藥性。
Prokesch和他的同事們還將HepG2細胞系進行體外培養,結果顯示,在模擬FMD的培養基中添加索拉非尼4小時后,細胞凋亡信號就已經升高;HepG2細胞的活力隨索拉非尼的劑量提高而降低,細胞毒性、細胞凋亡數量隨劑量提高而增加。這一結果,在患者來源耐藥性HCC類器官的體外培養中也再次得到證實。
總之,索拉非尼與FMD在治療HCC上具有協同作用,兩者聯合治療能破解HCC細胞對索拉非尼的耐藥性問題,提高療效。
從機制上看,索拉非尼是線粒體呼吸的非典型抑制劑,會導致癌細胞氧化磷酸化(OXPHOS)過程受損,使癌細胞轉為無氧呼吸,通過增強糖酵解來提供能量[9,10](也就是發生Warburg效應[11])。
糖酵解需要消耗大量葡萄糖。Prokesch和他的同事們在HepG2細胞的體外實驗中發現,索拉非尼治療后的癌細胞活力會隨葡萄糖劑量的增加而逐漸恢復。當培養基中葡萄糖濃度為3mM時,細胞活力還沒啥起色;當葡萄糖添加到5mM時,就有約50%的癌細胞恢復活力。
而在小鼠體內的異種移植實驗中,他們發現,FMD喂養的小鼠血糖水平顯著降低至約3mM。這說明,憑著FMD就足以將體內血糖降至一定水平,降低HCC細胞在使用索拉非尼后的存活率。
簡單來說就是,索拉非尼堵住HCC細胞有氧呼吸的路,轉型為糖酵解;而FMD又會導致HCC細胞的糖酵解也沒糖可用,從而聯手索拉非尼將HCC細胞逼向絕路。
研究者們進一步研究發現,FMD不僅能夠降低血糖,還能阻斷AKT/mTOR信號通路,增加HCC細胞對索拉非尼的敏感性。
值得注意的是,p53能夠通過調節葡萄糖轉運蛋白和促凋亡蛋白的表達,在FMD+索拉非尼的協同治療中起關鍵作用。
當敲除HepG2 細胞中的p53基因時,FMD與索拉非尼對HepG2 細胞的“合體攻擊”就失效,不會出現顯著的細胞活力降低或是細胞毒性加強。一旦p53重新表達,FMD就又能增加HepG2 細胞對索拉非尼的敏感性了。
相關新聞

